Edema maculare diabetico (DME) – Per i disturbi visivi legati la Commissione Europea ha approvato brolucizumab
“La Commissione Europea (CE) ha approvato brolucizumab 6 mg per il trattamento dei disturbi visivi dovuti a edema maculare diabetico (DME). Si tratta della seconda indicazione approvata dalla CE per brolucizumab, già approvato dal 2020 per il trattamento della degenerazione maculare umida legata all’età. La decisione della CE si applica a tutti i 27 Stati membri dell’Unione europea (UE), nonché a Islanda, Norvegia e Liechtenstein
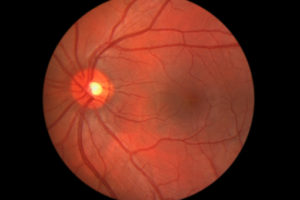 “L’edema maculare diabetico è una pericolosa manifestazione clinica della retinopatia legata al diabete. Colpisce dal 5 al 7% delle persone con diabete mellito, che sono purtroppo tantissime, oltre 4 milioni in Italia, un dato destinato a crescere in proporzione all’aumento della prevalenza della malattia – precisa Agostino Consoli, Ordinario di Endocrinologia, Università ‘G. d’Annunzio’ di Chieti, Responsabile della Uoc Territoriale di Endocrinologia e Malattie Metaboliche della Ausl di Pescara e Presidente della Società Italiana di Diabetologia (SID) – Nella retinopatia diabetica i vasi sanguigni, danneggiati dall’alta concentrazione di glucosio nel sangue, permettono la fuoriuscita di liquidi che si accumulano nella macula, causandone l’edema e portando col tempo a deficit visivi importanti. Ecco perché un trattamento con agenti anti-VEGF come il brolucizumab, molecole capaci di mantenere sotto controllo la fuoriuscita del fluido, risulta particolarmente efficace”.
“L’edema maculare diabetico è una pericolosa manifestazione clinica della retinopatia legata al diabete. Colpisce dal 5 al 7% delle persone con diabete mellito, che sono purtroppo tantissime, oltre 4 milioni in Italia, un dato destinato a crescere in proporzione all’aumento della prevalenza della malattia – precisa Agostino Consoli, Ordinario di Endocrinologia, Università ‘G. d’Annunzio’ di Chieti, Responsabile della Uoc Territoriale di Endocrinologia e Malattie Metaboliche della Ausl di Pescara e Presidente della Società Italiana di Diabetologia (SID) – Nella retinopatia diabetica i vasi sanguigni, danneggiati dall’alta concentrazione di glucosio nel sangue, permettono la fuoriuscita di liquidi che si accumulano nella macula, causandone l’edema e portando col tempo a deficit visivi importanti. Ecco perché un trattamento con agenti anti-VEGF come il brolucizumab, molecole capaci di mantenere sotto controllo la fuoriuscita del fluido, risulta particolarmente efficace”.
L’approvazione europea si basa sul primo anno primo anno degli studi di Fase III KESTREL e KITE, trial randomizzati e in doppio cieco, che hanno raggiunto l’endpoint primario di non inferiorità rispetto ad aflibercept nella variazione della acuità visiva meglio corretta (BCVA) rispetto al basale. In entrambi gli studi, dopo la fase di carico, oltre la metà dei pazienti (55,1% in KESTREL e 50,3% in KITE) nel gruppo di brolucizumab 6 mg è rimasta in un intervallo di somministrazione di 12 settimane durante il primo anno. Il dosaggio di aflibercept è allineato alle indicazioni Ue approvate nel primo anno di trattamento…”
Per continuare a leggere la news originale:
Fonte: “Edema maculare diabetico, approvazione europea per brolucizumab. Si dà ogni 8-12 settimane”, PHARMASTAR

