Malattie rare – Angioedema ereditario, Fda approva lanadelumab, primo inibitore callicreina
“La Food and Drug Administration degli Stati Uniti ha approvato lanadelumab, il primo farmaco del suo genere per il trattamento di pazienti di età pari o superiore a 12 anni affetti da angioedema ereditario, una rara malattia ereditaria che provoca edema. Il farmaco è un anticorpo monoclonale che ha come bersaglio la callicreina plasmatica
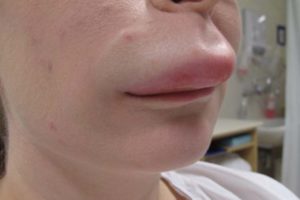
La Food and Drug Administration degli Stati Uniti ha approvato il primo farmaco del suo genere per il trattamento di pazienti di età pari o superiore a 12 anni affetti da angioedema ereditario, una rara malattia ereditaria che provoca edema della cute, delle mucose e degli organi interni. Tali edemi in alcuni casi possono anche essere fatali. Sviluppato da Shire sarà messo in commercio con il maerchio Takhzyro,
Precedentemente noto con il nome chimico di lanadelumab, l’anticorpo monoclonale, è stato approvato per il trattamento di pazienti con angioedema ereditario di tipo I e II (HAE), una malattia che colpisce circa 1 su 50.000 persone.
La malattia colpisce persone che hanno bassi livelli di una certa proteina e provoca episodi di grave gonfiore in diverse aree come lo stomaco, gli arti, il viso e la gola.
Lanadelumab è un anticorpo monoclonale che ha come bersaglio la callicreina plasmatica, coinvolta nell’eziopatogenesi dell’angioedema ereditario (HAE) o angioedema di Quincke, una malattia rara caratterizzata da gonfiore ricorrente della cute, delle mucose e degli organi interni che a volte può essere fatale.
Ci sono solo pochissimi farmaci per la cura degli attacchi di HAE e dei suoi sintomi e Shire ne possiede la maggior parte, disponendo di Cinryze (C1-inibitore umano), Firazyr (icatibant) e Kalbitor (ecallantide).
Nel 2015 Shire ha acquisito Dyax e con essa ha ottenuto il controllo di DX-2930, successivamente denominato lanadelumab, di particolare interesse per via del meccanismo d’azione che differisce da quello dei farmaci già disponibili.
L’appeal di lanadelumab deriva anche dal fatto che il farmaco ha un meccanismo di azione diverso rispetto ai farmaci già disponibili. A differenza di Cinryze, Kalbitor e di altri farmaci approvati per l’HAE – come Berinert (CSL Behring) e Ruconest (Salix)- lanadelumab non inibisce la C1 esterasi. Il farmaco si lega e ostacola la callicreina plasmatica.
COME AGISCE IL FARMACO Lanadelumab, un anticorpo monoclonale, inibisce l’azione della callicreina, bloccando potenzialmente la cascata che porta alla generazione di bradichinina.
RUOLO DEL SISTEMA DELLA CALLICREINA-CHININA L’angioedema ereditario è causato da mutazioni che riducono la produzione o l’espressione della proteina inibitore C1 – un enzima che inibisce l’attività delle proteine coinvolte nell’ infiammazione, coagulazione del sangue e altri sistemi. Senza l’azione della proteina C1 inibitore, il sistema carellicreina-chinina (Il sistema chinina–callicreina, o più semplicemente sistema delle chinine è un sistema poco caratterizzato di proteine del sangue, che svolge un ruolo nell’infiammazione, nel controllo della pressione arteriosa, nella coagulazione del sangue e nel dolore) non è inibito, con conseguente eccesso di produzione di bradichinina, che provoca perdita vascolare ed è responsabile del gonfiore osservato nei pazienti HAE.
La bradichinina è un neurotrasmettitore peptidico prodotto localmente nei tessuti dell’organismo…”
Per continuare a leggere la news originale:
Fonte: “Angioedema ereditario, l’Fda approva lanadelumab, il primo inibitore della callicreina”, PHARMASTAR

